核外电子排布与运动状态一、能层、能级和原子轨道1. 能层
能层是核外电子按能量差异划分的层次,对应原子结构示意图中的第一层、第二层等,符号为K、L、M、N等(n=1,2,3,4...)。离核越近,能层能量越低。
2. 能级
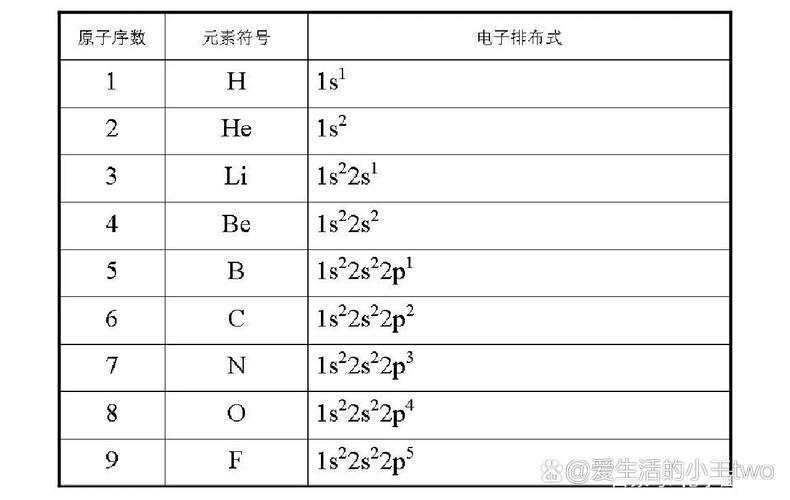
同一能层的电子能量存在微小差异,进一步分为不同能级,符号为s、p、d、f等。各能级的原子轨道数及最多容纳电子数如下:
二、原子轨道的形状、数目及能量1. 轨道形状2. 能量关系三、原子核外电子排布规律1. 一般规律2. 三大原理3. 稳定状态特例
全充满(p⁶、d¹⁰、f¹⁴)、半充满(p³、d⁵、f⁷)、全空(p⁰、d⁰、f⁰)状态能量更低,更稳定。例如:
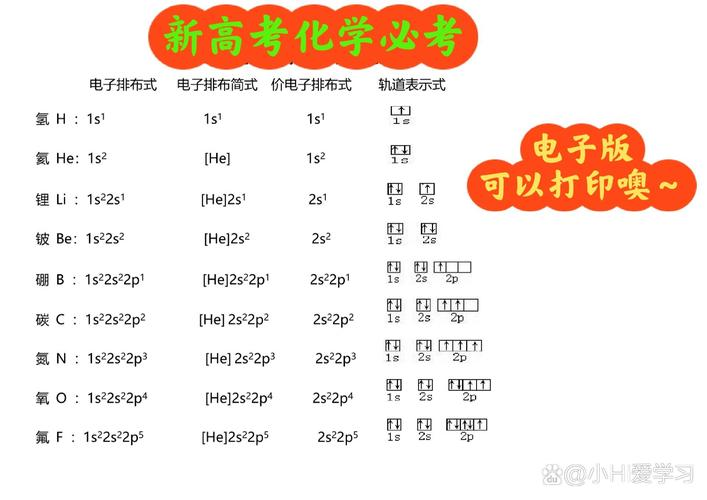
四、电子运动状态与空间运动状态1. 电子运动状态
核外每个电子的运动状态均不同,电子运动状态数=核外电子数。例如,氧原子(8个电子)有8种电子运动状态。
2. 空间运动状态

指电子占据的轨道数,空间运动状态数=轨道数。例如,氧原子电子排布为1s²2s²2p⁴,轨道数为1(1s)+1(2s)+3(2p)=5,故空间运动状态数为5。
五、典型元素/离子的电子排布实例1. 磷(P,15号元素)2. 铬(Cr,24号元素)3. 亚铁离子(Fe²⁺,26号元素Fe失去2个电子)4. 铜(Cu,29号元素)六、易错点与注意事项书写顺序:电子排布式中,(n-1)d能级写在ns前(如Fe:3d⁶4s²,而非4s²3d⁶)。 失电子顺序:过渡元素失电子时,优先失去ns电子(如Fe²⁺失去4s²电子,形成3d⁶)。 基态与激发态:基态原子能量最低,电子跃迁到高能级形成激发态(如基态Li:1s²2s¹,激发态可能为1s¹2s²)。 洪特规则特例:全充满、半充满、全空状态稳定,需牢记Cr、Cu等特例元素的排布。